第二节 蓄电池工作原理
蓄电池的工作过程就是化学能与电能的转换过程。放电时,蓄电池将化学能转换为电能供用电设备使用;充电时,蓄电池将电能转换为化学能储存起来备用。
蓄电池的单格电池是由浸渍在电解液中的正极板和负极板组成,电解液是硫酸水溶液。在蓄电池充放电过程中,发生的化学反应是可逆的。自1859年法国科学家加斯顿·普莱特发明铅酸蓄电池以来,关于蓄电池化学反应过程有各种不同的理论,一般认为格拉斯顿和特拉普于1882年创立的双极硫酸盐化理论(简称双硫化理论)能较确切地说明蓄电池的化学反应过程。
根据双硫化理论,铅蓄电池正极板上的活性物质是二氧化铅(Pb02),负极板上是海绵状铅(Pb),电解液是硫酸水溶液(H2SO4)。当蓄电池和负载接通放电时,正极板上的二氧化铅和负极板上的铅都将转变成硫酸铅(PbS04),电解液中的硫酸减少、相对密度下降。当蓄电池接通直流电源充电时,正、负极板上的硫酸铅又将分别恢复成原来的二氧化铅和纯铅,电解液中丽硫酸增加,相对密度增大。如果略去化学反应的中间过程,其化学反应方程式如下:

一、放电过程
将蓄电池的化学能转换成电能的过程称为放电过程,如图3-9(a)所示。
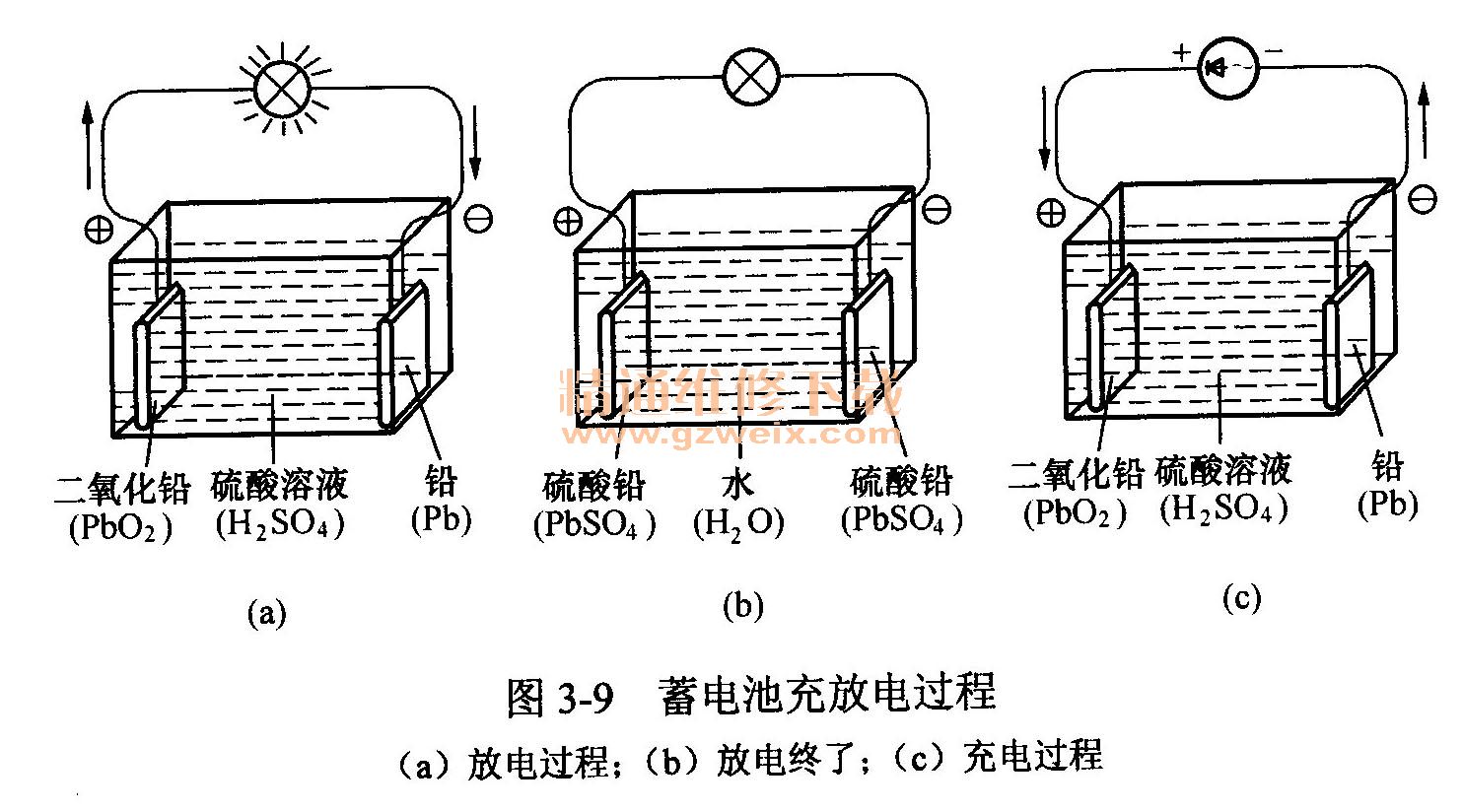
当放电尚未开始时,正极板是二氧化铅,负极板是纯铅,电解液是硫酸溶液。于正、负两极不同物质与电解液发生化学反应,使正极板具有正电位,约为2.0V;极板具有负电位,约为(-0.1) v。正、负两极间的电动势E为
E=2.0-(-0.1)=2.1(V)
当放电电路接通时,在电动势的作用下,电流便从正极流出,经过灯丝流回负极。电流流过灯丝会使灯丝发热,当电流足够大时,会使灯丝炽热而使灯泡发出亮光。
在放电过程中,由于正极板上的活性物质二氧化铅和负极板上的活性物质纯铅不断与电解液发生化学反应,因此二氧化铅和纯铅逐渐转变成硫酸铅,正极电位逐渐降低,负极电位逐渐升高,使正负极间的电位差逐渐降低;电解液中的硫酸成分逐渐减少、水分逐渐增多,使电解液密度逐渐减小。当电位差降低时,流过灯丝的电流就会减小,灯丝发热量相应减少,灯泡亮度变弱,直到不能发光为止,如图3-9(b)所示。
理论上,放电过程将进行到正负极板上的活性物质全部转变为硫酸铅为止。实际上,由于电解液不能渗透到活性物质最内层,因此所谓完全放电事实上只有20%~30%的活性物质转变为硫酸铅。要提高活性物质的利用率,就必须增大活性物质与电解液之间的反应面积。目前,常用措施有采用薄型极板和增大活性物质的孔率。
二、充电过程
将电能转换成蓄电池化学能的过程称为充电过程。充电时,蓄电池应接直流电源,电池正极接电源正极,电池负极接电源负极,如图3-9(c)所示。
将完全放电的蓄电池与直流电源接通时,电流就会按与放电时相反的方向流过蓄电池。此时蓄电池内部将发生与放电过程相反的化学反应,正、负极板上的硫酸铅将分别还原为二氧化铅和纯铅,电解液中硫酸成分逐渐增多而水分逐渐减少,电解液密度逐渐增大。
在充电过程中,上述化学反应不断进行,充电一直进行到极板上的活性物质完全恢复到放电前的状态为止。
在充电末期,电解液相对密度将升高到最大值,充电电流将用于电解水,所以在电解液中将产生大量气泡。
蓄电池充电终了的特征是:
(1)蓄电池内产生大量气泡,即出现沸腾现象。
(2)蓄电池端电压和电解液相对密度均上升至最大值,且在2~3h内不再增加。
第三节 蓄电池工作参数
蓄电池的主要工作参数有电解液的相对密度、电动势、端电压、电流、内阻、容量等。
一、相对密度
电解液的相对密度是指电解液中硫酸成分所占的比例。实测密度应按下式换算成25℃时的相对密度P25℃:
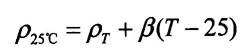
式中Ρt----实测电解液密度,g/cm3 ;
T----实测电解液温度,℃;
β----密度温度系数(β=0.0007),即温度每升高1℃ ,密度将降低0.0007g/cm3。
二、静止电动
蓄电池处于静止状态(不充电也不放电)时,正、负极板之间的电位差(即开路电压)称为静止电动势。静止电动势的高低与电解液的相对密度和温度有关,在密度为1.05~1.30g/cm,范围内,静止电动势ES可用下述经验公式计算,
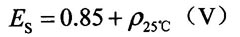
汽车用蓄电池电解液的密度在充电时增大,放电时减小,一般在1.12~1.30g/cm3变化,因此其静止电动势相应地在1.97~2.15V变化。
三、内阻
电流流过蓄电池时所受到的阻力称为蓄电池的内阻。蓄电池的内阻包括极板电阻、隔板电阻、电解液电阻、联条电阻和极柱电阻。在正常状态下,蓄电池的内阻很小,39所以能够供给几百安培甚至上千安培的起动电流。
极板电阻很小,且随极板上活性物质的变化而变化。充电时电阻变小,放电时电阻变大,特别是在放电终了时,由于活性物质转变成为导电性能较差的硫酸铅,因此电阻大太增加。
隔板电阻与材料有关。木质隔板多孔性差,所以电阻比微孔橡胶和塑料隔板的电阻大。此外,隔板越薄,电阻越小。
电解液的电阻与其温度和密度有关。如6-Q-75型蓄电池在温度为40℃时的内阻为0.010Ω,而在-20℃时,内阻则为0.019Ω,可见内阻随温度降低而增大。
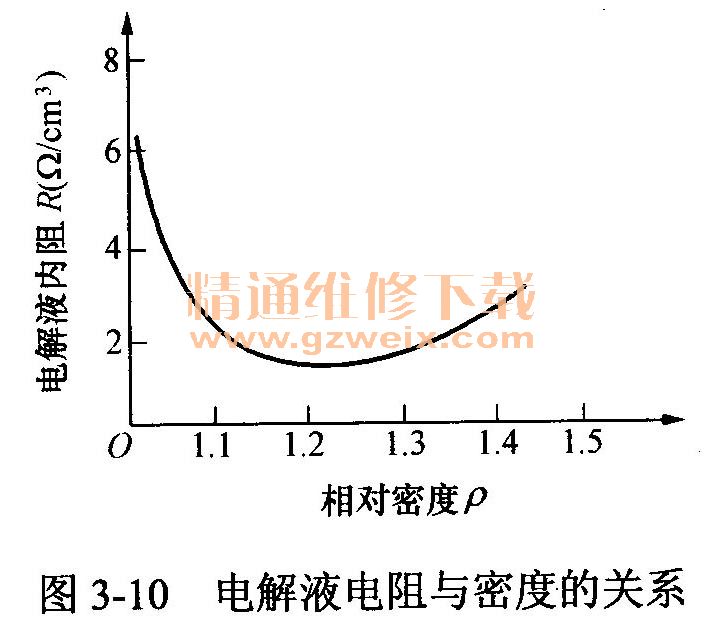
电解液电阻与密度的关系如图3-10所示。由图可见,电解液相对密度为1.20时,硫酸的离解度最好,黏度较小,所以电阻最小。
四、容量
1.容量概念
蓄电池的容量是指在规定的放电条件(放电电流、放电温度和终止电压)下,蓄电池能够输出的电量,用C表示。
当恒流放电时,蓄电池的容量等于放电电流与放电时间之积,即
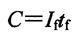
式中C----蓄电池容量,Ah;
If----放电电流A;
Tf----放电持续时间,h。
蓄电池容量是反映蓄电池对外供电能力、衡量蓄电池质量优劣以及选用蓄电池的重要指标。容量越大,可提供的电能越多,供电能力也就越大;反之,容量越小,则供电能力就越小。
蓄电池的容量与放电电流、电解液温度、放电终止电压和放电持续时间有关。因此,蓄电池出厂时规定的额定容量是在一定的电解液温度、一定的放电电流和一定的终止电压下测得的。GB 5008.1-2005《起动用铅酸蓄电池技术条件》规定,以20h放电率额定容量作为起动型蓄电池的额定容量。
2.额定容量
蓄电池的20h率额定容量是指完全充足电的蓄电池,在电解液温度为25℃±5℃条件下,以20h率的放电电流(即0.05C20安培电流)连续放电至12V蓄电池的端电压降到10.5V±0.05V时输出的电量,角C20表示,单位为Ah。
额定容量是检验蓄电池质量的重要指标。新蓄电池必须达到该指标,否则就为不合格产品。例如:对新产6-QA-105型蓄电池以5.25A电流连续放电至电压降到10. 5V±0.05V时,若放电时间大于或等于20h,则其容量为C=Iftf≥105Ah,达到或超过了额定容量105Ah,因此该蓄电池为合格产品;若放电时间小于20h,则其容量为C=Iftf<105Ah,低于额定容量值105Ah,因此该蓄电池为不合格产品。
3.储备容量
国际蓄电池协会和美国汽车工程师协会(SAE)规定:蓄电池容量用储备容量表示, GB 5008.1-2005对储备容量的定义和试验方法也有明确规定。
蓄电池的额定储备容量是指完全充足电的蓄电池,在电解液温度为25℃±5℃条件下,以25A电流连续放电至12V蓄电池电压降到10.5V±0.05V时,放电所持续的时间,用CM表示,单位为min。
储备容量表达了在汽车充电系统失效的情况下,蓄电池能为照明和点火系统等用电设备提供25A恒流的能力。例如,北京切诺基吉普车58-475型蓄电池的额定储备容量为82min; 6-QA-60型蓄电池的额定储备容量为94min。
第四节 影响蓄电池容量因素
蓄电池容量并不是一个固定不变的常数,而与很多因素有关,归纳起来分为两类:一类与生产工艺及产品结构有关,如活性物质的数量、极板的厚薄、活性物质的孔率等;另一类是使用条件,如放电电流、电解液温度和电解液相对密度等。
一、产品结构因素对蓄电池容量影响
1.极板上活性物质数量
从理论上讲,活性物质越多,则容量越大。要得到1Ah的电量,负极板上要有3.866g铅,正极板上要有4.463g二氧化铅,电解液中要有3.66g硫酸。实际上,正负极板上只有55%~60%的活性物质参加反应。
当活性物质的数量确定后,其他因素对容量的影响就是对活性物质利用率的影响了。极板面积越大,片数越多,则同时与硫酸起化学反应的活性物质就越多,容量就越大。国产蓄电池极板面积基本统一,每对极板面的容量为7.5Ah。
2.极板厚度
极板越厚,电解液向极板深处扩散就越困难,活性物质越不容易参与反应。因此,减小极板厚度可以提高活性物质的利用率。例如,采用厚度为1.7mm的薄型极板,蓄电池在相同体积的情况下,容量可以提高40%左右。
3.活性物质孔率
孔率是指活性物质孔隙的多少,孔率越大,硫酸溶液扩散渗透越容易,容量就可相应提高。但孔率过大时,活性物质的数量就会减少,容量反而会下降。
4.活性物质真实表面积
活性物质的真实表面积包括活性物质与电解液直接接触的表面积和细孔内的表面积。极板的真实表面积要比极板的几何尺寸计算面积大几百倍。真实表面积大,扩散面积和反应面积都会增加,容量就可相应提高。
5.极板中心距
极板中心距小,可以减小蓄电池的内电阻。因此,在保证有足够硫酸量的前提下,缩小极板中心距可以提高蓄电池的容量。
二、使用条件对蓄电池容量的影响
1.放电电流影响
蓄电池的放电特性是指在恒流放电过程中,蓄电池的端电压和电解液密度随时间而变化的规律。
由放电特性曲线可以看出,蓄电池放电后电解液密度是沿直线下降的。这是因为放电电流一定,则在单位时间内所消耗的硫酸量是相同的。所以随着放电时间的延长,电解液中的硫酸量会越来越少,根据实测结果,密度每下降0.04,蓄电池约放电25%.
放电过程中,蓄电池的端电压也是逐渐下降的。因为蓄电池内阻上有压降,所以端电压总是小于其电动势。其数学表达式为
U=E-IfR0
式中U----蓄电池端电压;
E----蓄电池电动势;
I f----放电电流;
R0----蓄电池内阻。
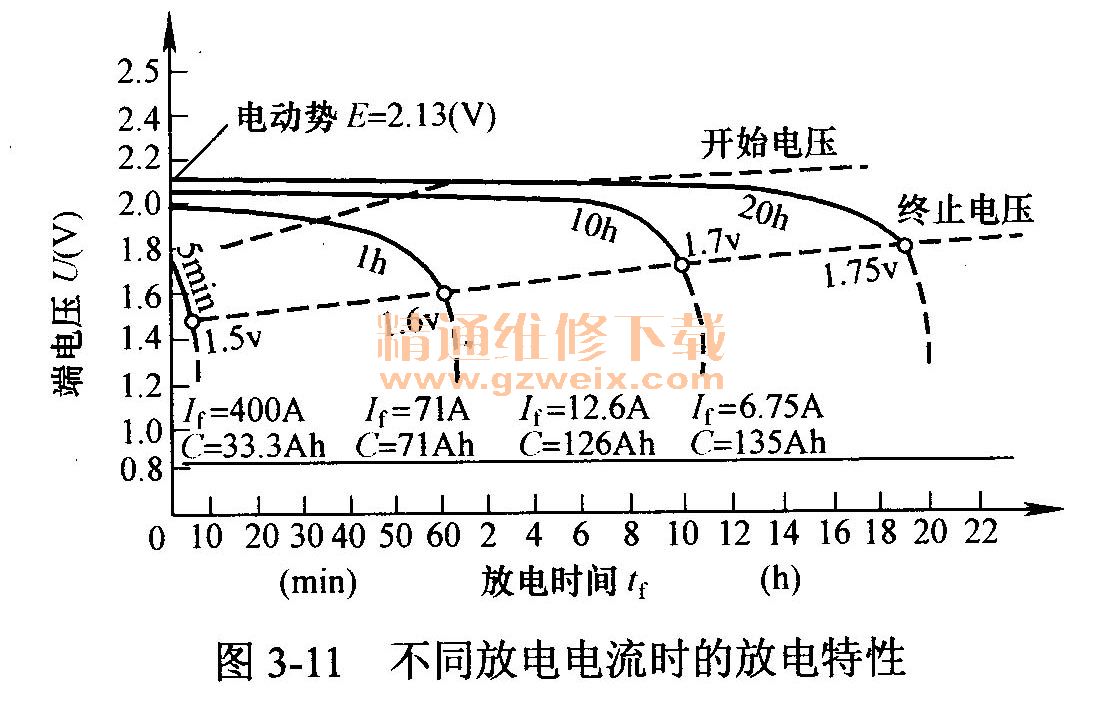
由图3-11所示为6-Q-135型蓄电池在不同放电电流情况下的放电特性可见,放电电流越大,电压下降越快,越容易出现放电“终了”的现象,放电开始单格电压便从2.1V迅速下降。当单格电压下降到1.75V时(20h率),应切断负载,停止放电。若再继续放电,电压将急剧下降,称为过度放电。过度放电会使硫酸铅的晶粒变大,充电时不仅不易还原,而且会堵塞极板孔隙使电解液渗透困难,造成蓄电池容量下降而影响蓄电池使用寿命。因此,在起动发动机时,必须严格控制起动时间,每次起动时间不得超过5s,再次起动应间隔15s以上。图3-12所示为3-Q-75型蓄电池在电解液温度为30℃时,蓄电池容量与放电电流的关系。

2.电解液温度影响
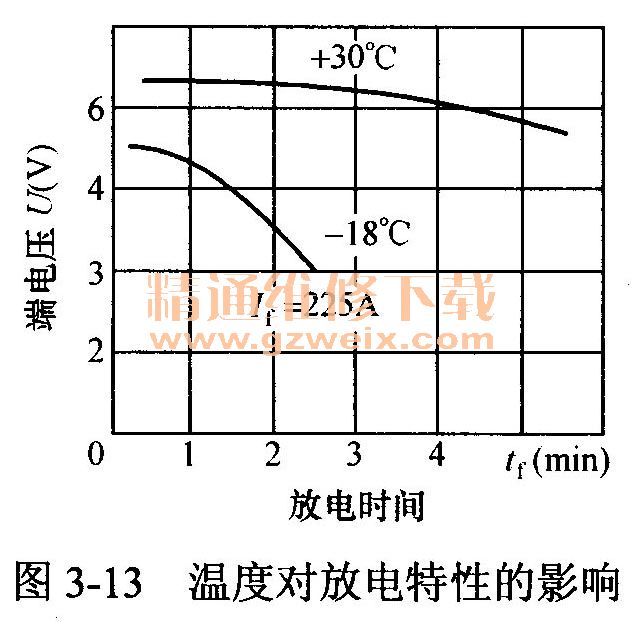
温度降低则容量减小,这是由于温度降低时,电解液的勃度增加,渗入极板内部困难,使离子扩散速度和化学反应速度降低;同时电解液电阻也增大,使蓄电池内阻增加,电动势消耗在内阻上的压降增大,蓄电池端电压降低,允许放电时间缩短,因此容量减小。图3-13所示为3-75型蓄电池电解液温度分别为+30℃和-18℃的情况下,以225A电流放电时的端电压与放电时间的关系。图3-14所示为3-Q-75型蓄电池以225A电流放电时,在不同温度条件下的输出容量。

GB/T 5008.1-2005规定,蓄电池额定容量是指电解液温度为25℃时的20h率容量。温度每降低1℃,缓漫放电时容量约减少1%,迅速放电时将减少2%。不同温度条件下的容量可用下式换算为25℃时的容量。
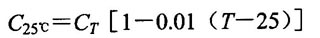
式中C25℃----换算为25℃时的容量,Ah;
CT----电解液平均温度为T时的实际容量,Ah;
T----放电终止时,中间单格电池电解液的温度,℃。
温度对蓄电池输出容量的影响给我国北方寒冷地区冬季汽车运行带来了一定的困难,因此冬季应注重蓄电池的保温工作。为了防止冬季温度低给车辆机动性能带来不利,军用车辆蓄电池采用了低温起动型蓄电池。如风帆蓄电池厂生产的6-QAJ-60型和6-QAJ-135型军用干荷电蓄电池,在-41℃条件下,能保证发动机顺利起动。
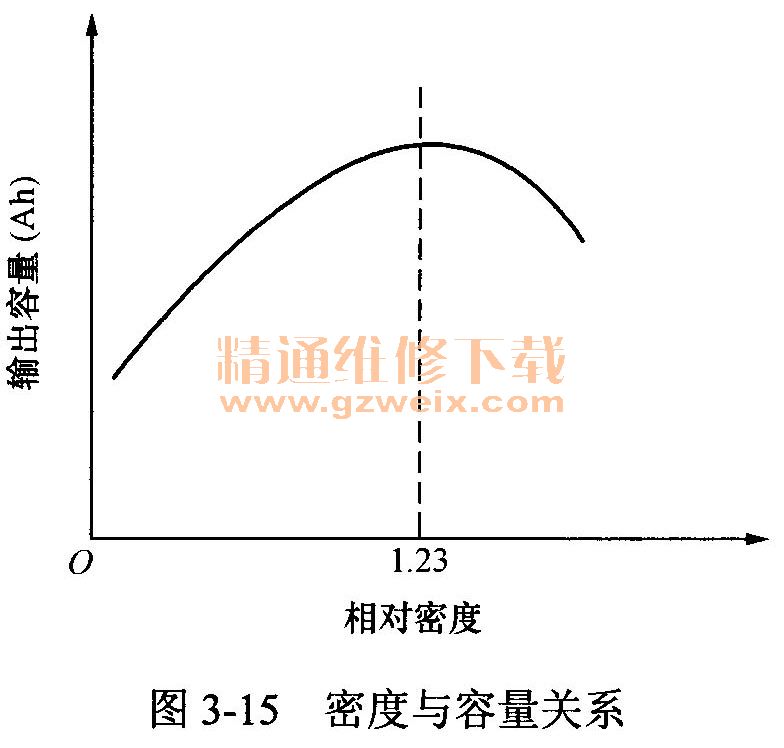
适当增大电解液密度,可以提高电解液个的渗透速度和蓄电池电动势,延长放电时间,从而提高蓄电池输出容量。但是,当密度超过一定值时,由于电解液豁度增大使浸透速度降低,内阻和极板硫化增加,因此蓄电池输出容量又会减小。试验证明,电解液相对密度约为1.23时,蓄电池输出容量最大,如图3-15所示。综合考虑电解液密度对蓄电池性能的影响,汽车用起动型蓄电池充足电时的电解液密度一般选在1.26~1.29范围内。
上一页 [1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] 下一页